Quando avviene una reazione chimica, è importante conoscere la velocità con cui essa avviene.
La velocità di reazione viene definita come il rapporto tra la concentrazione dei reagenti e l'intervallo di tempo in cui essa avviene, ovvero la quantità di sostanza che si trasforma nell'unità di tempo.
V= (ΔC)/(Δt)
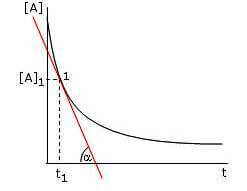
Il grafico a fianco mostra l'andamento della velocità di reazione in relazione alla concentrazione dei reagenti e del tempo.
Ovviamente a t= 0 s i reagenti avranno il valore massimo e quindi, con l'aumentare del tempo, diminuisce la loro concentrazione.
Per calcolare la velocità di reazione ad un determinato istante t, bisogna trovare il coefficiente angolare della retta tangente a quel punto sull'asse dei tempi. Più il valore dell'angolo sarà maggiore, maggiore sarà la velocità istantanea.
Consideriamo ora una reazione generica rappresenta nel grafico:
A+B - C+D
Dal grafico possiamo notare che con il diminuire della quantità di reagenti, aumenta contemporaneamente la concetrazione de prodotti; tuttavia i reagenti non si consumano fino ad esaurirsi.

Nessun commento:
Posta un commento