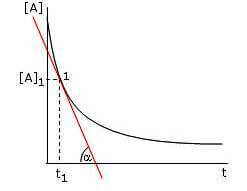
La velocità di reazione è influenza da diversi fattori.
Per far si che una reazione avvenga con successo, è necessario rompere i legami tra gli atomi delle molecole delle sostanze reagenti. Da ciò si puo' comprendere che la velocità di reazione è notevolmente influenzata dalla natura di questi legami; più essi sono forti e complessi, tanto la velocità della reazione sarà più lenta.
Al contrario le reazioni tra ioni sono più veloci, dal momento che il legame è molto debole.
- La concentrazione dei reagenti
Anche la concentrazione dei reagenti influisce sulla velocità di reazione. Infatti nelle reazioni omogenee (ovvero quelle in cui i reagenti si presentano in un'unica fase) la velocità di reazione è direttamente proporzionale alla concentrazione dei reagenti.
Consideriamo la reazione generale:
A+B- C+D
Si può dire la velocità con cui avviene una reazione è uguale al prodotto tra le concentrazioni dei reagenti elevate al proprio indice stechiometrico per la costante cinetica K.
Questa legge è chiamate "Equazione cinetica".
Un altro aspetto importante è l'Ordine di reazione, ovvero la somma degli esponenti dell'equazione cinetica.
L'aumento della temperatura fa aumentare l'energia cinetica delle particelle; quindi anche la velocità di reazione aumenterà.
- La presenza di Catalizzatori
Molte reazioni hanno la necessità di catalizzatori, ovvero di sostanze che accelerano la riuscita di una reazione. I catalizzatori vengono indicati come positivi, se la velocità aumenta; se, al contrario, la velocità diminuisce, allora vengono chiamati negativi o inibitori. Durante la reazione i catalizzatori non vengono coinvolti e, quindi, rimangono inalterati.